stimorolextra wrote:Kjemikern wrote:
Jeg prøver å tegne H-NMR-spekteret og får dette: en triplett (for CH3) og en dublett (for CH3) ca. ved 1 ppm. Men hvem skal ha lavest skift av disse? I tillegg får jeg en pentett (for CH2) ca ved 1,4 ppm, en hekstett (for CH) ca ved 1,6 ppm og en dublett (for OH) trolig ved høyeste skift, opp mot 6 ppm. Stemmer dette?
$CH_3-CH(OH)-CH_2-CH_3$
$CH_3$ er koblet til en $CH(OH)$ Denne $CH_3$ er mer skjermet av OH-gruppen. Så denne $CH_3$ molekylet vil ha et høyere skift enn $CH_3$ molekylet på andre siden, fordi den er koblet til $CH_2$ molekyl(H-atomet skjermer mindre enn OH).
Altså vil $CH_3$ lengst til venstre ha et skift på ca. 1.4ppm og den helt til høyre på ca 1. Og da er det helt riktig som du sier at den som er lengst til venstre er en dublett, mens den til høyre blir triplett.
$CH_2$ vil også være som du sier en pentett. Det er vanskelig å estimere ca skift, men som du sier så vil dette ligge høyere enn $CH_3$ molekylene, pga større skjerming(Skjermet av en $CH(OH)$ på den ene siden, og skjermet av $CH_3$ på den andre.
$CH$ molekylet er veldig godt skjermet ,Nesten like store sidekjeder på vær side! Så denne er som du sier veldig godt skjermet og vil derfor ha et høyt kjemisk skift, og vil opptre som en sekstett.
Og til slutt vil OH molekylet ha det høyeste skiftet, pga det sterk elektronegative O-atomet. H-atomet som er koblet til oksygenatomet vil være så godt skjermet at den vil ikke "se" noen naboer.
Et 1H-NMR spekter vill for dette molekylet se slikt ut :
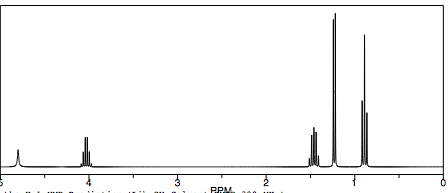
- Skjermbilde 2016-05-29 kl. 15.40.40.png (16.26 KiB) Viewed 10241 times

